 Brint (hydrogen)
Brint (hydrogen)
blev brugt i Montgolfiers ballon og i Döbereiners brintfyrtøj, hvor en
platinsvamp antænder en brintstrøm, når der åbnes for hanen til glasbeholderen,
hvor brinten udvikles af zink og syre.
Solen består af brint, der driver en
fusion, så helium dannes.
Tidligere blev det lavet ud fra vanddamp og jern, med et stort kulforbrug til
energiforbruget, men i dag er ZDANSKY metoden herskende, da lavtrykselektrolysen
er simpel med små anlægsudgifter og giver god indtjening, hvis man har billig
strøm til rådighed. Der er også tilgang til brint fra olie- og gasforekomsterne.

Fremstillingen af Brint i stor stil sker bedst gennem elektrolysemetoden, der også giver ilt.
I laboratoriet har man typisk det her (tv.) viste apparat når man skal bruge større mængder brint til forsøg.
De 2 haner i siderørene åbnes og der påfyldes vand, så siderørene er fyldt helt op. Hanerne lukkes og der sættes strøm til anode og katode, så luftarterne begynder at boble op, efterhånden som vandet spaltes af strømmen. Fra slanger der er sat på hanerne kan man nu lede luftarterne til tanke til oplagring. Man kan rense luftarterne og komprimere dem eller anvende dem direkte til en lang række kemiske processer hvorved kostbare kemikalier og fødevarer fremstilles. For at fremstille fast fedtstof som margarine fra flydende olier anvendes det og for at omdanne ringere olietyper til mere brugbart benzin osv.
Lærebøgerne starter med at fortælle at brint (hydrogen) er et af de vigtigste stoffer i et samfund da så mange produkter hidrører herfra. Gennem den kemiske industri eller import har Danmark tidligere måtte skaffe brint, men en helt ny epoke vil indledes med brintfremstillingen fra overskydende vindkraft når forbrugerne ikke bruger strøm om natten. Fordi man ikke har brugt denne mulighed tidligere har især lande med vandkraft stået for fremstilling af brint gennem elektrolyse. Med tilgang af billigt råstof som strøm vil en række nye produkter lavet v.hj.a. brint være mere konkurrencedygtige og dermed attraktive at indlede produktionen af. Også Ilt kan måske bruges på nye måder med den lavere pris.
Brint er så vigtigt fordi store mængder vigtige råvarer laves af brint. Det er først og fremmest ammoniak gennem Haber-Bosch metoden, idet det laves til kunstgødning i meget store mængder, hvilket også udleder CO2 gennem produktionens energiforbrug, hvis den sker ud fra kul og olie. Vi har her som eksempel en af Danmarks forsyndelser i det industrifråds, der har bragt kloden til katastrofens rand (og det inden de fattige fik del i overforbruget).
Et lille exempel på samspillet mellem råvaretilgang og udvikling af rene teknikker: Til minedrift o.a. anvendes vanligvis sprængstoffer fremstillet af ammoniak, men med mulighed for lokal fremstilling af ilt udover brinten, kunne man tænke sig, at nye ideer vil vinde indpas som fx. anlæg til on site fremstilling af miljørigtige sprængstoffer til minedrift, hvilket iøvrigt har den fordel at man undgår transport og oplagring af store mængder af resourcekrævende og sprængfarlige emner, idet porøst træstof som kork kan imprægneres med ilt og anvendes ved sprængningen, hvis det anvendes inden ilten slipper bort. Man kan altså ikke gemme sprænglegemerne, men man må lave dem på stedet. Fordelen er også et bedre arbejdsmiljø for minearbejderne der undgår indånding af kvælstofoxider fra de nitrater som almindeligvis anvendes. Også klor kan laves af overskudsstrømmen, hvilket kunne være grundlag for især saltsyrefremstilling, men også de mange anvendte klorprodukter som kloropløsninger og klor i fast form.
Den helt store anvendelse af brint er til fremstilling af ammoniak, da dette
jo indeholder dels bundet kvælstof, men også -brint. Kvælstof fra luften og
brint laves først til ammoniak
(v.h.j. af 2-300 atm. tryk og katalysator). Ammoniak kan med ilt (og
katalysator) omdannes til salpetersyre, der ved blanding med ammoniak giver
kunstgødning. Med fosfor fra slagteriaffald, som benmel og andet kan fås
fosfatgødning, der med ammoniak giver ammoniumfosfatgødning, hvorved planten får
både nitrat- og fosfatgødning fra blandinger af ammoniumnitrat og -fosfat.
Kalium fås fra kaliumsulfat. Den tidligere store danske produktion findes ikke
mere, trods endog god rentabilitet i produktionen og de samfundsmæssige fordele
af en national produktion af de produkter der er de industrielt vigtigste efter
olien.
Brint anvendes til fremstilling af bl.a. saltsyre.
Det har haft en stor anvendelse i fremstillingen af kunstigt benzin og har i
dag stor betydning indenfor kemisk behandling af ringere olietyper, for at
producere lettere olietyper af større værdi som netop benzin og kan bruges til
metanfremstilling. Billigere brint ville kunne forlænge olieresurserne til nogle formål.
Indenfor vegetabilsk olie har det også stor betydning alene til
margarineproduktionen og fremstilling af fast fedtstof til industriel friture,
bageri osv.
Det bruges udbredt i metalforarbejdningsprocedurer som jern og zink og i en
række processer med jod, brom, fluor, svovl og mange andre. Bruges til
fremstilling af halvmetaller og hydrider.
En stor værdi er at det kan bruges som hjælp til at fremstille meget rene
stoffer som metaller uden kul, ilt og metaller hidrørende fra en råvare.
Laboratoriefremstilling
industriel fremstilling
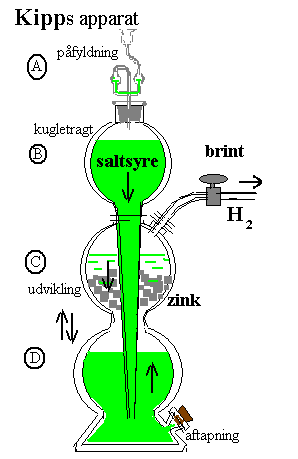
Herunder er vist et traditionelt laboratorieglasapparat, der kan levere brinten
når det ønskes, men som kan afbrydes ved at lukke hanen, så syren fortrænges fra
metallet og udviklingen ophører indtil hanen igen åbnes så syren på ny stiger op
over metallet og gasudviklingen så begynder igen.
|
Elektrolysen:
H2O >
2H + O

Den kemiske industri anvender meget brint, ofte i bunden form f.x.som
syre
H + Cl > HCl (saltsyre)osv.
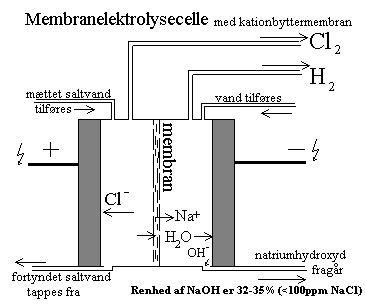
Chlor laves typisk på samme måde i elektrolysecelle med
saltvand.

BT KEMI
Teckomatorp
|
Udsendelse
Brintsamfundet
Brint(hydrogen) er et godt alternativ til olie og naturgas
Fremstillingen af Brint i stor stil sker bedst gennem elektrolyse, der også giver ilt.

Elektrolyseceller
under 2. verdenskrig i Norge. Strømmen stammer fra vandkraft.

Med syre laves bl.a. en lang række af salte, fx. til kunstgødning
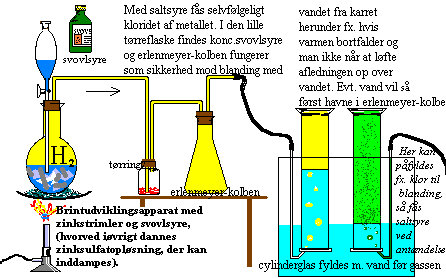
medicin, metaludvinding og som hjælpestoffer i kemiske processer. |
 Brint (hydrogen)
Brint (hydrogen) 







